Forschungsthemen
Elektronenspinresonanz
Die Elektronenspin-Resonanz (engl. electron paramagnetic resonance, EPR) gehört zusammen mit der bekannteren Kernspin-Resonanz (engl. nuclear magnetic resonance, NMR) zu den Methoden der magnetischen Resonanz.
Beide Methoden beruhen auf der Ausrichtung des Spins (Elektronen- oder Kernspin) in einem äußeren Magnetfeld und der Möglichkeit, durch elektromagnetische Strahlung entsprechender Wellenlänge (Mikrowelle in der EPR, Radiofrequenz in der NMR) zwischen diesen Einstell-Möglichkeiten Übergänge zu induzieren. Wir verwenden Methoden der EPR-Spektroskopie, um folgende Fragestellungen zu bearbeiten:
Hydrogenasen
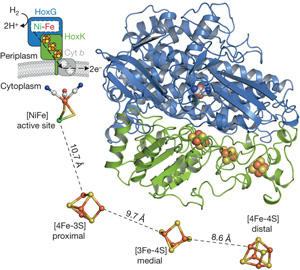
Fritsch et al., Nature 479:249-252, 2011
Die reversibel biokatalytische Spaltung von molekularem Wasserstoff in Protonen und Elektronen ist in der mikrobiellen Welt weitverbreitet und wird durch das Metalloenzym Hydrogenase katalysiert. Die hier untersuchten Enzyme ist eine Untergruppe der H2-spaltenden Biokatalysatoren, der sogenannten O2-toleranten [NiFe]-Hydrogenasen, welche auch unter atmosphärischer O2-Konzentration einen normalen H2-Umsatz aufrecht erhalten können.
Unser Ziel ist ein grundlegendes Verständnis der O2-Toleranz der Hydrogenasen in Ralstonia eutropha, die membrangebundene Hydrogenase (MBH), die lösliche Hydrogenase (SH) und die regulatorische Hydrogenase (RH) werden hierfür individuell untersucht, aber auch hinsichtlich der Gemeinsamkeiten und Unterschiede untereinander und im Vergleich zu Standardhydrogenasen. Durch die Anwendung fortschrittlicher EPR-spektroskopischer Methoden wie FT-EPR, ENDOR, ESEEM und HYSCORE wollen wir die elektronischen Strukturen der Metallkofaktoren aufklären und sie mit strukturellen Motiven in Verbindung bringen, wie sie z.B. in der kürzlich gelösten Kristallstruktur der MBH auftreten. Im Fokus stehen das Wildtypprotein und Varianten mit relevanten Änderungen im katalytischen Zentrum und in der Elektronentransferkette. Studien an Einkristallen werden dazu beitragen, spezielle Wechselwirkungen zwischen Metall-Clustern und Protein zuzuordnen. Die Experimente werden unter verschiedenen Redoxbedingungen durchgeführt, um die einzelnen, mittels EPR sichtbaren, Schritte im katalytischen Zyklus zu beobachten. Zusätzlich werden wir durch Experimente an Varianten von Maturationsprodukten zum Verständnis des Aufbaus des Proteins beitragen, der Schwerpunkt liegt hier auf den FeS-Clustern. Parallel dazu wird von uns die Entwicklung von in-situ-EPR-Spektroskopie an ganzen Zellen voran getrieben, um spezifische zytoplasmatische Bedingungen mit einzelnen Redoxzuständen der Kofaktoren in den Hydrogenasen in Zusammenhang zu bringen.
Dieses Projekt ist Teil des Forschungsbereichs E3 innerhalb von UniCat und beinhaltet die Zusammenarbeit mit den Gruppen von P. Hildebrandt (IR/Raman), O. Lenz (Biochemie von Metalloenzymen), M. Kaupp (Theorie), M. A. Mroginski (Theorie), sowie P. Scheerer (Kristallographie).
Kontakt: Christian Teutloff
Mitarbeiter: Julia Löwenstein
In-Cell EPR unter Verwendung von Mikroresonatoren
Kontakt: Christian Teutloff
Mitarbeiter: Andrey Pivtsov
Aktivierung von Kohlendioxid
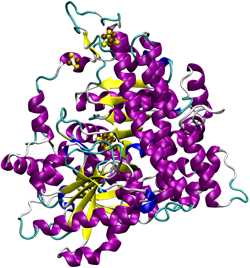
Der globale Kohlenstoffkreislauf hängt von der biologischen Umsetzung von Kohlenstoffoxiden ab, welche den reduktiven Einbau von CO2 in organische Moleküle (z.B. in der Photosynthese und anderen autotrophen Pfaden), die direkte Reduktion von CO2 zu CO oder Format, die Oxidation von CO zu CO2 und den C-C Bindungsaufbau durch Reaktion von CO mit einem Methylkation zur Bildung einer Azetylgruppe umfässt. Drei ausgewählte Molybdän-Enzymklassen werden untersucht: die Mo-enthaltende CO-Dehydrogenase (Mo-CODH), Formatdehydrogenasen (FDH) und drei Enzyme aus dem reduktiven Azetyl-Koenzym-A Pfad: die Ni,Fe-enthaltende CO-Dehydrogenase (Ni,Fe-CODH), die Azetyl-CoA-Synthase (ACS) und das Corrinoid-Eisen/Schwefel Protein (CoFeSP).
Die katalytischen Zentren der zwei CODHs und ACS sind heterobimetallisch und die zwei Metalle Co und Ni sind am entscheidenden Schritt zur Bildung aktivierter Essigsäure von einer Cobalt-gebundenen Methylgruppe im CoFeSP und dem Nickel-gebundenen CO am ACS beteiligt.
Die zwei Hauptziele unserer Untersuchungen sind (A) zu verstehen wie die Metallzentren und die Proteinumgebung zur Aktivierung und Umsatz von Kohlestoffoxiden beitragen und (B) Wege zur Ausnutzung dieser Reaktivität in optimierten Enzymvarianten und Komplexen zu entwickeln. Alle ausgewählten enthalten Metallbindungsstellen, welche einzigartig in der Natur sind. Die Rolle der einzelnen Metalle und ihr Wechselspiel miteinander soll aufgeklärt werden.
Innerhalb dieses Forschungsprojekts werden wir verschiedenen EPR-Techniken auf die paramagnetischen Zustände in Ni, Fe-enthaltenden CODHs, ACS und CoFeSP, als auch den Mo-enthaltenden CODHs und den FDH anwenden. Dabei zielen wir auf die Aufklärung des katalytischen Mechanismus, indem die erhaltenen Informationen über die elektronische und geometrische Struktur der katalytischen Zentren verknüpft werden sollen, spezieller in substratgebundenen Zuständen. Besonderer Fokus wird auf Zustände gerichtet sein, für welche noch keine Kristallstruktur existiert. Die dafür erforderlichen EPR- und ENDOR-Experimente werden in enger Zusammenarbeit mit den Gruppen von S. Leimkühler und H. Dobbek durchgeführt.
Dieses Projekt ist Teil des Exzellenzclusters "Unifying Concepts in Catalysis", Projektbereich E2
Kontakt: Christian Teutloff
Protonentransfer in Channelrhodopsin
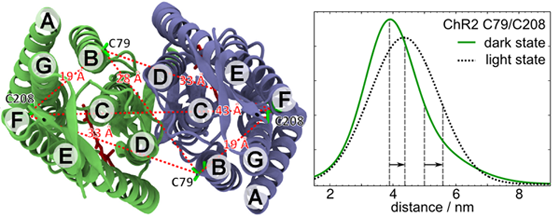
Wir untersuchen Strukturveränderungen und Änderungen des Wasserstoffbrücken-Netzwerkes des licht-aktivierten Ionenkanals Channelrhodopsin (ChR) mit Hilfe ortsspezifischer Spinmarkierungen und verschiedener EPR-Methoden. Die mit EPR detektierbaren Parameter an ein Protein gebundener Spinmarkierungen reagieren sehr empfindlich auf die Umgebung des Labels und können somit dazu genutzt werden, Veränderungen in der Polarität und Wasserstoff-Verbrückung des Proteins zu erkennen. Desweiteren verwenden wir gepulste Elektron-Elektron Doppelresonanz (ELDOR) um strukturelle Veränderungen des ChR während des Photozyklus zu erkennen.
Diese Projekt wird im Rahmen des SFB 1078 (Projekt B4) von der Deutschen Forschungsgemeinschaft gefördert.
Kontakt: Robert Bittl
Mitarbeiter: Christopher Engelhard
Photorezeptoren
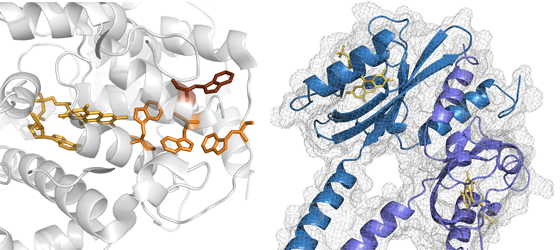
Einen weiteren bedeutenden Teil unserer Forschungsinteressen stellen biologische Photorezeptoren dar. Zusätzlich zu unserer SFB-geförderten Forschung an Channelrhodopsin gibt es in diesem Bereich noch zwei weitere Forschungsschwerpunkte:
Elektronentransfer in Cryptochromen
Cryptochrome sind eine Klasse von Blaulicht-empfindlichen Proteinen bei denen vermutet wird, dass sie einen Anteil an der Magnetfeld-Sensorik von Vögeln haben. Ihr Funktionsmechanism beruht vermutlich auf der Bildung eines Radikalpaares, welches sehr gut in der EPR charakterisiert werden kann. In unserer Forschung konzentrieren wir uns auf die Art und funktionale Bedeutung der Elektronentransferpfade, die zur Bildung des Radikalpaares führen, sowohl in vivo mit Hilfe von hochempfindlicher cw EPR, als auch in vitro mit Hilfe von transienter, zeitaufgelöster EPR.
Dieses Projekt ist Teil einer Kooperation mit Dr. Margaret Ahmad an der Universität von Paris, Frankreich.
Der Signalmechanismus von LOV-Domänen
LOV-Domänen sind eine Klasse von Blaulichtrezeptoren, die in der Natur nahezu ubiquitär sind. Sie sind für die Forschung von besonderem Interesse, da sie an sehr viele verschiedene Effektordomänen binden können. Unser Fokus ist die Untersuchung des Signalmechanismus, der dieses modulare Verhalten ermöglicht. Dazu verwenden wir sowohl ortsspezifische Spinmarkierungen als auch den Flavin-Kofaktor als intrinsische Spinsonde für ELDOR und ENDOR Doppelresonanz-Spektroskopie.
Dieses Projekt ist Teil einer Kooperation mit Prof. Andreas Möglich von der Humboldt Universität zu Berlin und Prof. Wolfgang Gärtner am Max-Planck Institute for Chemical Energy Conversion in Mülheim, Deutschland.
Kontakt: Robert Bittl
Mitarbeiter: Christopher Engelhard
Gadolinium-haltige Kontrastmittel für MRT
Der Sonderforschungsbereich 1340 "Matrix in Vision" untersucht am Beispiel von Entzündungsprozessen, wie die extrazelluläre Matrix (EZM) in der medizinischen Bildgebung genutzt werden kann. Für eine Reihe klinisch relevanter inflammatorischer Krankheiten sollen neue Bildgebungssonden untersucht werden sowie deren Wechselwirkung mit der EZM. Hierbei werden molekularbiologische Methoden in der Radiologie mit biophysikalischen Untersuchungen kombiniert, um die Wechselwirkung der Bildgebungssonden mit der EZM zu verstehen, neue Bildgebungsverfahren zu evaluieren sowie eine quantitative Bildgebung zu entwickeln.
Die Magnetresonanztomographie (MRT) ist eine mächtige bildgebende Methode in der Medizin, die ein wertvolles Hilfsmittel in der medizinischen Diagnostik darstellt. Manchmal ist die Nutzung von venös verabreichten Kontrastmitteln notwendig, um den Kontrast für spezifische Gewebe zu erhöhen. Der Einsatz von gadoliniumhaltigen Kontrastmitteln ist hierbei sehr erfolgreich, weil Gd3+ vorteilhafte paramagnetische Eigenschaften hat, die eine hohe Kontrastverstärkung liefern.
Ungebundenes Gd3+ ist sehr toxisch und kann zu ernsthaften Gesundheitsproblemen führen (M. Rogosnitzky et al., BioMetals 29, 365–376 (2016)), deswegen wird dessen Toxizität in Kontrastmittelkomplexen durch Chelatisierung minimiert. Dennoch können leider einige der Komplexe dissoziieren und das freigesetzte Gd3+ kann im Gewebe verbleiben bzw. angereichert werden (S. J. George et al., Brit. J. Dermat. 163, 1077–1081 (2010)).
Medizinisch hochrelevant ist es, die Komplexdissoziation der Kontrastmittel und neue Gd3+ Bindungsstellen in Körpergeweben zu untersuchen. Aufgrund des Elektronenspins des Gd3+ (S=7/2) eignet sich die Elektronenspin-Resonanspektroskopie (EPR) als Untersuchungsmethode in ihren unterschiedlichen Facetten (z.B. cw-EPR, gepulste EPR, Doppelresonanzmethoden) sehr gut. Damit kann die lokale Umgebung des Gd3+-Ions untersucht werden. Es ist z.B. möglich, die Art der Nachbarionen zu bestimmen (soweit diese magnetische Eigenschaften haben), wie auch die Distanzen zu diesen. Darüber hinaus ist es möglich, Information über die Art der Ligandierung des Gd3+ abzuleiten.
Unterschiede in der lokalen Umgebung des Gd3+ (z. B. durch unterschiedliche Liganden) kann man über Veränderungen der Nullfeldaufspaltung verfolgen. Diese Änderungen sollen über EPR in einem Multifrequenzansatz verfolgt werden. Außerdem können die Hyperfeinwechselwirkung von Gd3+ mit Kernen wie H, N oder S, Elektron-Elektron Wechselwirkungen und T1/T2-Relaxationszeiten benutzt werden, um zwischen verschiedenen Bindungsstellen zu unterscheiden.
In diesem Projekt arbeiten wir mit unterschiedlichen Probentypen (von Modellsubstanzen über Zellen bis hin zu verschiedenen Geweben). Wir vermessen die Proben in einem weiten Magnetfeldbereich (0-6 T) und mehreren Mikrowellenfrequenzen (4, 9, 34, 94 GHz) bei verschiedenen Temperaturen (von 5 K bis Raumtemperatur).
Für Interessierte haben wir laufend Themen für Bachelor- und Master-Arbeiten. Bitte kontaktieren Sie uns für weitere Information.
Diese Projekt wird im Rahmen des SFB 1340 (Projekt A03) von der Deutschen Forschungsgemeinschaft gefördert.
Kontakt: Christian Teutloff
Mitarbeiterin: Daria Dymnikova
Spinabhängiger Transport in Dünnschichtsilizium-Solarzellen
![]()
Der Wirkungsgrad von Dünnschichtsolarzellen auf der Basis von hydrogenisiertem amorphem und mikrokristallinem Silizium wird auf vielfältige Weise durch Defektzustände, Verunreinigungen und lichtinduzierte strukturelle Veränderungen im Absorbermaterial beschränkt. Ziel des interdisziplinären Forschungsnetzwerks „EPR-Solar“ war und ist es, ein detailliertes Verständnis dieser Defekte bezüglich ihrer nanoskopischen Struktur, ihrer Entstehung sowie ihrer Beteiligung an elektronischen Prozessen wie Transport und Rekombination in Solarzellen zu erarbeiten, um die Entwicklung geeigneter Maßnahmen zur Beseitigung dieser Defekte zu unterstützen.
Der Schwerpunkt der Tätigkeiten an der Freien Universität Berlin liegt im Bereich der Defektcharakterisierung sowie der Methodenentwicklung auf dem Gebiet der elektrisch detektierten magnetischen Resonanz Spektroskopie sowie der Elektronen paramagnetischen Resonanz Spektroskopie. Auf diesem Gebiet arbeiten wir eng mit dem Forschungszentrum Jülich, der TU München, dem Max-Planck-Institut für Eisenforschung in Düsseldorf sowie dem Helmholtz-Zentrum Berlin zusammen.
Kontakt: Jan Behrends
Mitarbeiter: Christoph Meier
Transport in Organischen Solarzellen
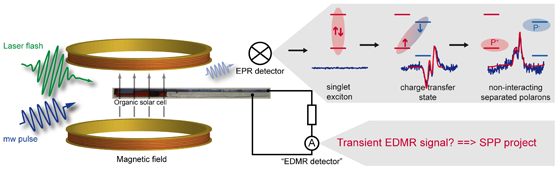
Wir beschäftigen uns damit, ein grundlegendes Verständnis von Ladungstransfer und Ladungstransport in organischen Solarzellen zu erarbeiten. Zu diesem Zweck werden passende EPR-basierte Techniken verwendet. Insbesondere soll die experimentelle Methode der transienten elektrisch detektierten magnetischen Resonanz (transiente EDMR) entwickelt werden. Die Kombination der Empfindlichkeit von EDMR und der Zeitauflösung von transienter EPR wird es uns ermöglichen, den Zusammenhang zwischen Ladungstransferkomplexen, die infolge von Photoanregung und anschließendem Ladungstransfer zwischen Donator und Akzeptor entstehen, und dem Photostrom von Polymer:Fulleren-Solarzellen systematisch zu untersuchen.
Dieses Projekt ist Teil des DFG Schwerpunktprogramms 1601 zum Thema “New Frontiers in Sensitivity für EPR Spectroscopy: From Biological Cells to Nano Materials”.
Kontakt: Jan Behrends
Mitarbeiter: Felix Kraffert
Ladungstrennung in Hybrid-Solarzellen

Hybrid-Solarzellen aus organischen und anorganischen Halbleitern bieten das Potenzial für zukünftige photovoltaische Bauelemente mit hohen Wirkungsgraden bei vergleichsweise niedrigen Produktionskosten. Die Kombination aus (nanostrukturierten) anorganischen Halbleitern und organischen Halbleitern erscheint besonders vielversprechend, da sich die Vorteile von beiden Materialien kombinieren lassen. Dennoch liegen die Wirkungsgrade derzeitiger Hybrid-Solarzellen in der Regel weit unterhalb der Wirkungsgrade von rein anorganischen Solarzellen bzw. Zellen mit ausschließlich organischen Absorbermaterialien. Ein entscheidender Grund hierfür ist oftmals die ineffiziente Ladungstrennung, d.h. die Umwandlung von photogenerierten Exzitonen in freie Elektronen und Löcher an der Hybrid-Grenzfläche. An dieser Stelle setzen unsere Arbeiten an.
In einem arbeitsgruppenübergreifenden Projekt (AG Weinelt / AG Bittl) im Rahmen der FU Focus Area “NanoScale” untersuchen wir die Prozesse an der Hybrid-Grenzfläche zwischen kristallinem Silizium und kleinen organischen Molekülen auf mikroskopische Ebene. Unser Ziel ist es, Strategien zur Verbesserung von Ladungstransfer und -trennung zu entwickeln.
Im Rahmen einer Helmholtz Energie-Allianz arbeiten wir gemeinsam mit dem Helmholtz-Zentrum Berlin, dem Forschungszentrum Jülich, der Humboldt-Universität zu Berlin und der Universität Potsdam daran, „Anorganisch/organische Hybrid-Solarzellen und -Techniken für die Photovoltaik“ zu entwickeln. Unser Schwerpunkt liegt dabei auf dem Erstellen eines umfassenden Verständnisses der Prozesse, die zur Exzitonendissoziation und Ladungsträgertrennung an Grenzflächen zwischen anorganischen Halbleitern (ZnO, CIGS, Si) und konjugierten organischen Polymeren bzw. kleinen organischen Molekülen führen.
Kontakt: Jan Behrends
Mitarbeiter: Robert Steyrleuthner